OpenText Documentum Content Management for Life Sciences
GxP-konformes Content Management in den Biowissenschaften sicherstellen
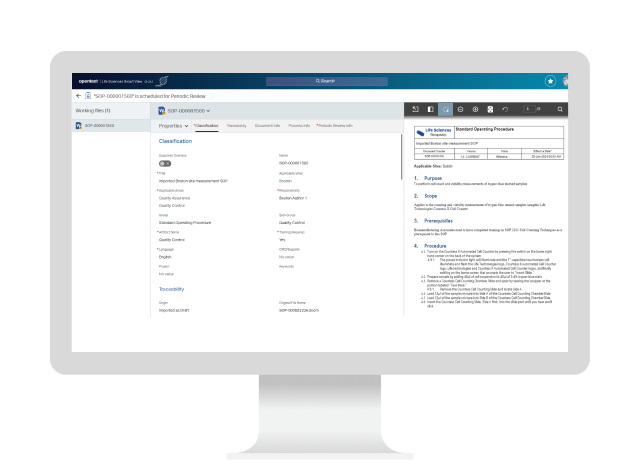
Beschleunigen Sie Ihr Geschäft mit intelligenter DokumentenverwaltungHolen Sie sich das IDC Market Spotlight!
Übersicht

Wie OpenText Documentum CM for Life Science für Unternehmen von Nutzen sein kann
Erfahren Sie mehr über die Vorteile von Documentum for Life Sciences.
-
Passen Sie sich durch Cloud-native Software an
Nutzen Sie eine containerisierte Architektur für einfache Upgrades und den Zugriff auf neue Funktionen und Updates – On-Premises, in einer hybriden Umgebung oder in der Cloud.
-
Stellen Sie eine einzige zentrale Quelle für regulierte Content bereit
Nutzen Sie mehrere Lösungsmodule in einem einzigen Repository für bereichsübergreifende Suchvorgänge und Verknüpfungen und vermeiden Sie so unnötige Importe und Exporte zwischen Systemen.
-
Verringern Sie Compliance-Risiken
Gewährleisten Sie mit Prüfprotokollen, Lebenszyklusverwaltung und der Zugriffs- und Versionskontrolle die Einhaltung der Vorgaben nach FDA 21 CFR Part 11. Setzen Sie Genehmigungsprozesse mit automatischen Zuweisungen durch.
-
Steigern Sie die Produktivität
Nutzen Sie branchenübliche Geschäftsprozesse für die Dokumentenkategorisierung, Lebenszyklen und Workflows für Pharmazeutika und medizinische Geräte, die die unternehmensweite Dokumentenkontrolle durchsetzen und gleichzeitig die Produktivität vor Ort verbessern.
-
Fördern Sie konforme, sichere Zusammenarbeit
Sie können Content und Prozesse gemeinsam mit internen und externen Mitarbeitern, autorisierten Partnern und anderen Dritten bearbeiten und wiederverwenden, ohne die Sicherheit und Compliance zu beeinträchtigen.
-
Vereinfachen Sie die Integration
Integrieren Sie die Lösung in die bestehende Infrastruktur, in On-Premises Systeme und in eine beliebige Cloud, darunter auch Systeme für Qualitätsmanagement, Lernmanagement und Enterprise Resource Planning.
Profitieren Sie von den Services von OpenText und Partnern
Dienstleistungen
OpenText Professional Services kombinieren End-to-End-Lösungsimplementierung mit umfassenden Technologiedienstleistungen zur Systemoptimierung.
- Holen Sie sich einen zuverlässigen Partner für Ihr Information ManagementIhr Weg zum Erfolg
- Bringen Sie Ihr Unternehmen mit modernen Lösungen in die ZukunftNextGen-Dienste
- Beschleunigen Sie Ihren Weg zum Information ManagementConsulting Services
- Schöpfen Sie das volle Potenzial Ihrer Informationsmanagement-Lösung ausCustomer Success Services
Partner
OpenText unterstützt Kunden bei der Suche nach der passenden Lösung, dem passenden Support und dem passenden Ergebnis.
- Durchsuchen Sie das Partnerverzeichnis von OpenTextPartner suchen
- Branchenführende Unternehmen, die OpenText-Produkte und -Lösungen ergänzenStrategische Partner
- Durchsuchen Sie den Katalog für OpenText-PartnerlösungenApplication Marketplace
Communitys
Lernen Sie unsere OpenText-Communities kennen. Knüpfen Sie Kontakte mit Einzelpersonen und Unternehmen, um Einblicke und Unterstützung zu erhalten. Nehmen Sie an Diskussionen teil.
Premium Support
Optimieren Sie den Wert Ihrer OpenText-Lösung mit engagierten Experten, die geschäftskritischen Support für Ihre komplexe IT-Umgebung bieten.